هل تساءلت يوماً عن المجموعة الواسعة من المعادن التي يتكون منها عالمنا؟ في هذه المدونة الرائعة سنبدأ في رحلة لاستكشاف الأنواع المختلفة من المعادن، من الشائع إلى النادر. سيرشدك مهندسنا الميكانيكي الخبير إلى الخصائص والتطبيقات الفريدة لكل معدن، مقدماً لك رؤى ستجعلك تشعر بالاندهاش. استعد لاكتشاف عالم من عجائب المعادن!

صُنِّفت قائمة المعادن التالية باستخدام طرق مختلفة. كما ذكرنا سابقًا، هناك أكثر من 90 نوعًا مختلفًا من المعادن الموجودة على كوكبنا.
يمكنك تنزيل نسخة PDF من هذه القائمة في أسفل الجدول.
| الفئة | المعادن |
|---|---|
| المعادن الحديدية | الحديد، والكروم، والمنغنيز |
| المعادن غير الحديدية | الألومنيوم، المغنيسيوم، البوتاسيوم، الصوديوم، الصوديوم، الكالسيوم، السترونتيوم، الباريوم، النحاس، النحاس، الرصاص، الزنك، القصدير، الكوبالت، النيكل، النيكل، الأنتيمون، الزئبق، الكادميوم، البزموت، الذهب، الفضة، البلاتين، الروثينيوم، الروديوم، الروديوم، البلاديوم، الأوزميوم، الإيريديوم، البريليوم، الليثيوم، الروبيديوم، الروبيديوم، السيزيوم، التيتانيوم، الزركونيوم، الزركونيوم، الهافنيوم، الفاناديوم النيوبيوم والتنتالوم والتنغستن والموليبدينوم والغاليوم والإنديوم والثاليوم والثاليوم والجرمانيوم والرينيوم والرينيوم واللانثانوم والسيريوم والبراسيوديميوم والنيوديميوم والنيوديميوم والسماريوم واليوروبيوم والجادولينيوم والتيربيوم والديسبروسيوم والديسبروسيوم والهوليميوم والإربيوم والإربيوم والثوليوم والإيتربيوم واللوتيتيوم والسكانديوم والسليكون والبورون والسيلينيوم والتيلوريوم والزرنيخ والثوريوم |
| المعادن الشائعة | الحديد، والألومنيوم، والنحاس، والزنك |
| المعادن النادرة | الزركونيوم، والهافنيوم، والنيوبيوم، والتنتالوم |
| المعادن الخفيفة | التيتانيوم، والألومنيوم، والمغنيسيوم، والمغنيسيوم، والبوتاسيوم، والصوديوم، والكالسيوم، والسترونتيوم، والباريوم (الكثافة <4500 كجم/م³) |
| المعادن الثقيلة | النحاس والنيكل والكوبالت والرصاص والرصاص والزنك والقصدير والأنتيمون والبزموت والكادميوم والزئبق (الكثافة > 4500 كجم/م³) |
| المعادن الثمينة | الذهب، والفضة، ومعادن المجموعة البلاتينية |
| العناصر الفلزية | الجرمانيوم، والأنتيمون، والبولونيوم |
| المعادن النادرة | المعادن الخفيفة النادرة (الليثيوم، والروبيديوم، والسيزيوم)، والمعادن الخفيفة النادرة (الزركونيوم، والموليبدينوم، والتنغستن)، والمعادن النادرة المشتتة (الغاليوم، والإنديوم، والجرمانيوم، والثاليوم)، والمعادن الأرضية النادرة (السكانديوم، والإيتريوم، وسلسلة اللانثانيد)، والمعادن المشعة (الراديوم، والفرانسيوم، والبولونيوم، واليورانيوم، والثوريوم) |
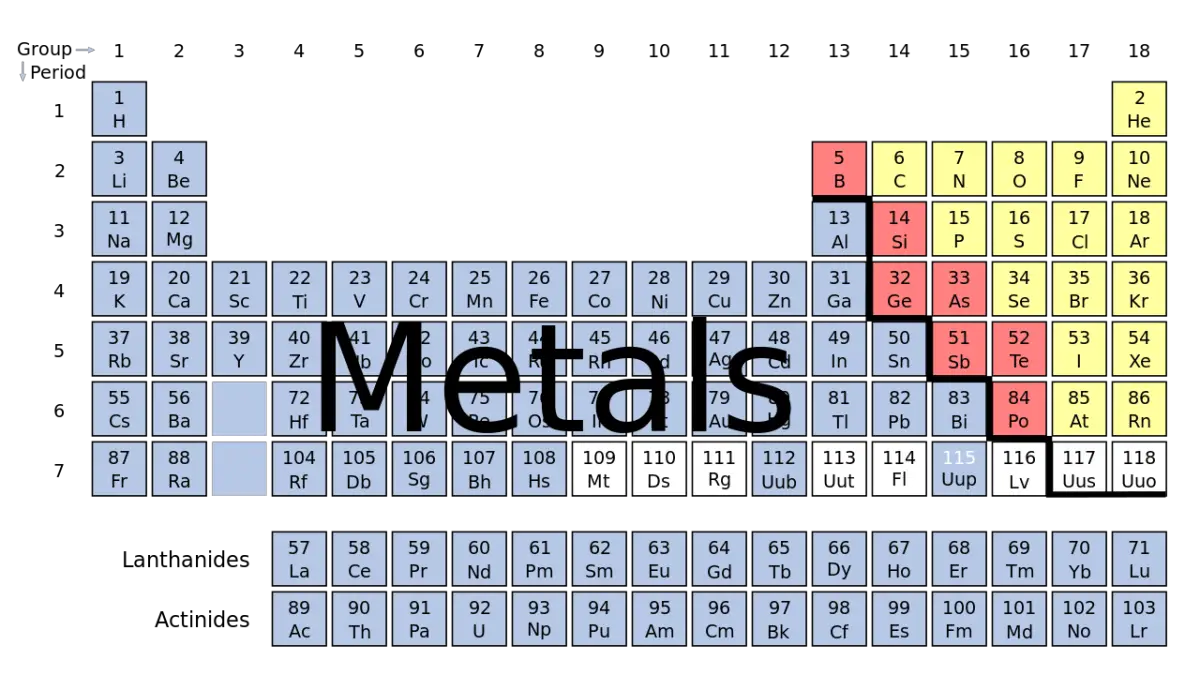
قد يكون فهم العدد الإجمالي للفلزات الموجودة أمرًا معقدًا للغاية نظرًا لاتساع نطاق العناصر. حتى الآن، هناك ما مجموعه 118 عنصرًا معروفًا في الجدول الدوري، منها 90 عنصرًا تقريبًا مصنفة على أنها فلزات. يتضمن ذلك ثلاثة عناصر يشار إليها عادة باسم أشباه الفلزات أو أشباه الفلزات، وهي البورون والسيليكون والزرنيخ.
لتبسيط الفهم، تنقسم المعادن عادةً إلى فئتين رئيسيتين: المعادن الحديدية وغير الحديدية. وهذا النظام التصنيفي مقبول على نطاق واسع في الولايات المتحدة وبريطانيا واليابان.
المعادن الحديدية
تحتوي المعادن الحديدية على الحديد وهي معروفة بقوتها ومتانتها. وتشمل الأمثلة الشائعة ما يلي:
المعادن غير الحديدية
لا تحتوي المعادن غير الحديدية على الحديد وعادةً ما تكون أكثر مقاومة للصدأ والتآكل. وتشمل الأمثلة على ذلك:
قراءة ذات صلة: المعادن الحديدية مقابل المعادن غير الحديدية
في الماضي، قام الاتحاد السوفيتي السابق وبعض دول أوروبا الشرقية بتصنيف المعادن إلى مجموعتين بناءً على لونها: المعادن السوداء والمعادن الملونة. وبالمثل، لا يزال هذا التصنيف القائم على اللون مستخدمًا في الصين. ومع ذلك، يفتقر هذا النهج إلى الصلاحية العلمية.
يتم تصنيف المعادن الآن بناءً على خصائصها وتطبيقاتها في أربع مجموعات متميزة:
المعادن الثقيلة:
تُعرف المعادن الثقيلة بأنها المعادن التي تزيد كثافتها عن 4.5 جم/سم مكعب. وتشمل الأمثلة على ذلك:
المعادن الخفيفة:
المعادن الخفيفة ذات كثافة أقل من 4.5 جم/سم مكعب. وتشمل الأمثلة على ذلك:
المعادن الثمينة:
المعادن الثمينة ذات قيمة عالية لانخفاض مستويات شوائبها، وعمليات تنقيتها المعقدة، وقيمتها العالية. وتعتبر هذه المعادن أكثر قيمة من المعادن العادية. ومن الأمثلة على ذلك:
المعادن النادرة:
تشمل المعادن النادرة عناصر غير شائعة نسبيًا، مثل المعادن الخفيفة النادرة والمعادن الحرارية النادرة والمعادن المشتتة والمعادن الأرضية النادرة. وتشمل الأمثلة ما يلي:
المعادن المشعة:
من المهم ملاحظة أن هناك أيضًا فئة من المعادن المشعة التي يمكن أن تكون ضارة بصحة الإنسان. يمكن أن يؤدي التعرض الطويل لهذه المعادن إلى المرض أو حتى الموت. ومن الأمثلة على ذلك:
الخاتمة
تهدف هذه المقالة إلى تقديم قائمة شاملة لأنواع مختلفة من الفلزات، تغطي جميع العناصر الموجودة في الجدول الدوري للعناصر الكيميائية تقريبًا. علاوة على ذلك، سنقدم لمحة شاملة عن خصائص هذه الفلزات وتطبيقاتها.
لنبدأ.

الحديد هو عنصر فلزي عدده الذري 26 ويمثله الرمز الكيميائي Fe، المشتق من اسمه اللاتيني "Ferrum". ويبلغ متوسط كتلته الذرية النسبية 55.845 وحدة كتلة ذرية (amu). ويُعد الحديد أحد أكثر العناصر وفرة على الأرض ويلعب دوراً حاسماً في العديد من التطبيقات الصناعية، لا سيما في إنتاج الصلب.
يُعد الحديد ضرورياً في العديد من المجالات نظراً لتعدد استخداماته ووفرة إنتاجه. فهو مكون أساسي في صناعة الصلب، وهو سبيكة من الحديد والكربون. ويُعد الفولاذ أساسيًا في مجالات البناء والسيارات ومختلف الصناعات الأخرى نظرًا لقوته ومتانته.

الكروم هو عنصر فلزي ينتمي إلى المجموعة 6B في الجدول الدوري للعناصر، ورمزه الكيميائي Cr وعدده الذري 24. واسمه مشتق من الكلمة اليونانية التي تعني "اللون"، ويرجع ذلك إلى الطبيعة الملونة لمركبات الكروم.
هذا المعدن الرمادي الصلب هو أقسى معدن موجود في الطبيعة. لا يوجد الكروم إلا بكميات صغيرة في القشرة الأرضية، حيث يحتل المرتبة السابعة عشرة من حيث الوفرة عند 0.011 تيرابايت 3 تيرابايت فقط. والكروم الحر الطبيعي نادر للغاية ويوجد بشكل أساسي في الكروميت.

المنجنيز هو فلز انتقالي رمزه الكيميائي Mn ورقمه الذري 25. يظهر كعنصر أبيض مائل للرمادي، صلب، هش ولامع.
في حين أن المنجنيز النقي أكثر ليونة قليلاً من الحديد، إلا أنه يصبح صلباً وهشاً عندما يحتوي على كميات صغيرة من الشوائب ويمكن أن يتأكسد بسهولة في البيئات الرطبة.
يتوزع المنجنيز على نطاق واسع في الطبيعة، حيث تحتوي التربة عادةً على حوالي 0.251 تيرابايت 3 طن من هذا العنصر. تحتوي بعض الأطعمة، مثل الشاي والقمح والفاكهة ذات القشرة الصلبة، على كميات أعلى من المنجنيز.

الألومنيوم، الذي يرمز له بالرمز Al، هو معدن خفيف أبيض فضي اللون قابل للسحب يستخدم عادةً في صناعة منتجات مختلفة مثل القضبان والصفائح والرقائق المعدنية والمسحوق والشرائط والخيوط.
في الهواء الرطب، يمكن أن يشكل الألومنيوم طبقة أكسيد تحمي من التآكل. عند تسخينه في الهواء، يمكن لمسحوق الألومنيوم أن يشتعل، مما ينتج عنه لهب أبيض ساطع. وهو قابل للذوبان في المحاليل المخففة لحمض الكبريتيك وحمض النيتريك وحمض الهيدروكلوريك وهيدروكسيد الصوديوم وهيدروكسيد البوتاسيوم، ولكنه غير قابل للذوبان في الماء.
وتبلغ الكثافة النسبية للألومنيوم 2.70، وتبلغ درجة انصهاره ودرجة غليانه 660 درجة مئوية و2327 درجة مئوية على التوالي.
وتجدر الإشارة إلى أن الألومنيوم هو العنصر المعدني الأكثر وفرة في القشرة الأرضية، ويحتل المرتبة الثالثة بعد الأكسجين والسيليكون.

المغنيسيوم هو عنصر فلزي يمثله الرمز الكيميائي Mg. وقد أنتجه الكيميائي البريطاني السير همفري ديفي لأول مرة في عام 1808 عن طريق اختزال أكسيد المغنيسيوم مع البوتاسيوم.
وباعتباره فلزاً قلوياً ترابياً، فإن المغنيسيوم معدن أبيض فضي خفيف، ويتميز بخصائص كيميائية تفاعلية. فهو يتفاعل مع الأحماض لإنتاج الهيدروجين ويتمتع ببعض الليونة وقدرات تبديد الحرارة.
يتوفر المغنيسيوم بوفرة بشكل طبيعي وهو عنصر أساسي لجسم الإنسان.

البوتاسيوم فلز قلوي يرمز له بالرمز K والعدد الذري 19. ينتمي إلى المجموعة 1أ من الدورة الرابعة في الجدول الدوري للعناصر.
يتميز هذا المعدن الشمعي الناعم والشمعي بمظهره الأبيض الفضي ويمكن قطعه بسهولة بالسكين. له درجة انصهار وغليان منخفضة وكثافة أقل من الماء. يُظهر البوتاسيوم خواص كيميائية تفاعلية عالية، حتى أكثر من الصوديوم.
الصوديوم، المعروف أيضًا برمزه Na واسمه الشائع صوديوم، هو عنصر فلزي يقع في المجموعة 1أ من الدورة الثالثة من الجدول الدوري. وهو ممثل لعناصر الفلزات القلوية.
يتميز الصوديوم بقوام ناعم ويظهر خواص كيميائية شديدة التفاعل. عندما يتلامس مع الماء، يتفاعل بقوة لإنتاج هيدروكسيد الصوديوم وإطلاق غاز الهيدروجين.

الكالسيوم عنصر فلزي عدده الذري 20 ورمزه Ca. يقع في المجموعة 2A والدورة الرابعة من الجدول الدوري للعناصر.
في درجة حرارة الغرفة، يكون الكالسيوم مادة صلبة بيضاء فضية اللون ذات خواص كيميائية تفاعلية عالية. ونظراً لتفاعليته، فإنه يوجد بشكل أساسي في الطبيعة في صورة أيونات أو مركبات.

السترونتيوم هو عنصر كيميائي يحمل الرمز Sr، اكتشفه الكيميائي والطبيب البريطاني السير هنري هوب في عام 1791-1792 أثناء دراسته لأحد الخامات. وقد أطلق عليه اسم السترونتيوم (تراب السترونتيوم) نسبة إلى مكان منشأه، وهو سترونتيان.
السترونتيوم هو فلز ترابي قلوي أبيض فضي اللون ذو بريق أصفر. ويستخدم في إنتاج السبائك والخلايا الضوئية والكواشف الكيميائية التحليلية والألعاب النارية وغيرها من التطبيقات.
أحد نظائره، وهو السترونتيوم-90، مشع ويبلغ عمره النصفي 28.1 سنة، مما يجعله مفيدًا كمصدر إشعاعي.

الباريوم هو عنصر فلز ترابي قلوي رمزه الكيميائي Ba، ويقع في المجموعة 2أ من الدورة السادسة في الجدول الدوري. وهو فلز أبيض فضي ناعم ذو مظهر لامع وهو العنصر الأكثر تفاعلية بين الفلزات القلوية الترابية.
نظرًا لطبيعته التفاعلية العالية، لا يوجد الباريوم في الطبيعة في شكله النقي. وبدلًا من ذلك، فإن أكثر معادن الباريوم شيوعًا الموجودة في الطبيعة هي الباريت (كبريتات الباريوم) والويذريت (كربونات الباريوم)، وكلاهما غير قابل للذوبان في الماء.
وعلى الرغم من الاعتراف بالباريوم كعنصر جديد في عام 1774، إلا أنه لم يُصنَّف كعنصر فلزي إلا بعد اختراع التحليل الكهربي في عام 1808.
تُستخدم مركبات الباريوم في الألعاب النارية لإنتاج اللون الأخضر بناءً على مبدأ تفاعل اللهب.

النحاس هو عنصر انتقالي وفلز رمزه الكيميائي Cu ورقم ذري 29.
النحاس في شكله النقي هو معدن ناعم ذو لون أحمر برتقالي وبريق معدني عند قطعه حديثاً. ويكون شكله العنصري أحمر مائل إلى البنفسجي.
النحاس مطيل للغاية ويتميز بتوصيل حراري وكهربائي ممتاز. ونظراً لهذه الخصائص، فإنه يستخدم على نطاق واسع في المكونات الكهربائية والإلكترونية، وكذلك الكابلات. كما يمكن استخدامه أيضاً في مواد البناء ويمكنه تشكيل العديد من السبائك، بما في ذلك البرونز والنحاس الأصفر، والتي تتميز بمقاومة منخفضة وخصائص ميكانيكية ممتازة.
النحاس معدن متين يمكن إعادة تدويره عدة مرات دون أن يفقد خواصه الميكانيكية.
قراءة ذات صلة: أنواع النحاس الأصفر

الرصاص هو عنصر كيميائي فلزي يرمز له الرمز Pb والرقم الذري 82 والوزن الذري 207.2. وهو أثقل العناصر غير المشعة وله بنية بلورية مكعبة متمركزة الوجه. والرصاص معدن ثقيل غير حديدي مقاوم للتآكل.
ويتمتع الرصاص بالعديد من المزايا، بما في ذلك نقطة انصهار منخفضة، ومقاومة عالية للتآكل، وعدم قابلية الاختراق للأشعة السينية وأشعة جاما، واللدونة الجيدة. وبسبب هذه الخصائص، تتم معالجته عادة في صفائح وأنابيب ويستخدم في صناعات مختلفة، مثل التصنيع الكيميائي وإنتاج الكابلات وتصنيع البطاريات والحماية من الإشعاع.

الزنك عنصر كيميائي يرمز له الرمز Zn والعدد الذري 30. ينتمي إلى المجموعة 12 من الدورة الرابعة في الجدول الدوري للعناصر. الزنك معدن انتقالي رمادي فاتح وهو رابع أكثر المعادن استخداماً في الصناعة الحديثة. وهو معدن أساسي في إنتاج البطاريات.

يشار إلى العنصر الفلزي المعروف باسم ستانوم عادةً باسم القصدير باللغة الإنجليزية، ورمزه العنصري هو Sn.
القصدير هو مادة غير عضوية تظهر عادةً على شكل معدن منخفض نقطة الانصهار مع بريق أبيض فضي، في أكثر أشكاله شيوعاً، القصدير الأبيض.
في المركبات، قد يُظهر القصدير تكافؤ إما اثنين أو أربعة، ولا يتأكسد بسهولة في الهواء في درجة حرارة الغرفة.
ويتواجد القصدير بشكل طبيعي في المقام الأول في شكل ثاني أكسيد (الكاسيتيريت) وكبريتيدات مختلفة، مثل كبريتيد الستانيك.
قراءة ذات صلة: أنواع القصدير

الكوبالت، الذي يرمز له بـ Co، هو فلز مغناطيسي حديدي ذو سطح أبيض فضي ولون وردي قليلاً. ويقع في المجموعة الثامنة والدورة الرابعة من الجدول الدوري، ويبلغ عدده الذري 27 ووزنه الذري 58.9332.
يحتوي الكوبالت على بنية بلورية سداسية سداسية متقاربة ويمكن أن يكون له عادةً تكافؤ +2 و+3. وهو معدن لامع لونه رمادي مائل إلى الصلب، وهو معدن صلب وهش نسبياً ومغناطيسي حديدي ويفقد مغناطيسيته عند تسخينه إلى 1150 درجة مئوية. وفي درجة حرارة الغرفة، يكون خاملًا للماء وثابتًا في الهواء الرطب.
عند تسخينه لدرجات حرارة أعلى من 300 درجة مئوية في الهواء، يخضع أكسيد الكوبالت (CoO) للأكسدة ويتحول إلى أكسيد الكوبالت (Co3O4) مع حرارة بيضاء ساطعة. يمكن لمسحوق معدن الكوبالت الناعم، الناتج عن اختزال الهيدروجين، أن يحترق تلقائيًا إلى أكسيد الكوبالت في الهواء.
يُعد الكوبالت مادة خام أساسية تُستخدم في تصنيع السبائك المقاومة للحرارة والسبائك الصلبة والسبائك المضادة للتآكل والسبائك المغناطيسية وأملاح الكوبالت المختلفة.

والنيكل معدن صلب وقابل للسحب ومغناطيسي حديدي يمتلك لمعاناً عالياً ومقاومة ممتازة للتآكل. وهو عنصر حديدي ويوجد بوفرة في لُب الأرض الذي يتألف في المقام الأول من الحديد والنيكل. ومحتوى النيكل في الصخور الحديدية المغنيسية في القشرة الأرضية أعلى من محتوى الصخور الألومينيزيليكية. على سبيل المثال، يحتوي البيريدوتايت على محتوى نيكل أعلى 1000 مرة من محتوى الجرانيت، بينما يحتوي الجابرو على 80 ضعف محتوى الجرانيت من النيكل.

الأنتيمون هو عنصر فلزي رمزه الكيميائي Sb ورقمه الذري 51. وهو معدن أبيض فضي لامع وصلب وهش يمكن تشكيله على هيئة قضبان وكتل ومسحوق وأشكال أخرى. يحتوي الأنتيمون على بنية بلورية متقشرة ويفقد بريقه بمرور الوقت عند تعرضه للهواء الرطب. وعند تعرضه لدرجات حرارة عالية، يحترق إلى أكسيد الأنتيمون الأبيض. الأنتيمون قابل للذوبان في أكوا ريجيا وحمض الكبريتيك المركز. وتبلغ كثافته النسبية 6.68 ودرجة انصهاره 630 درجة مئوية ودرجة غليانه 1635 درجة مئوية. وبالإضافة إلى ذلك، يبلغ نصف قطره الذري 1.28 أنجستروم، وسالبته الكهربية 2.2.

يُرمز إلى الزئبق بالرمز الكيميائي Hg، وهو العنصر رقم 80 في الجدول الدوري وينتمي إلى المجموعة 12 والدورة السادسة.
ما يجعل الزئبق فريداً من نوعه هو أنه الفلز الوحيد الذي يوجد في شكل سائل في درجة الحرارة والضغط العاديين. ومع ذلك، فإن الغاليوم (الرمز Ga، العنصر 31) والسيزيوم (الرمز Cs، العنصر 55) يوجدان أيضاً كسائلين في درجة حرارة الغرفة (29.76 درجة مئوية و28.44 درجة مئوية على التوالي).
يتميز الزئبق بمظهر أبيض فضي لامع وهو سائل كثيف ذو خواص كيميائية مستقرة. وهو غير قابل للذوبان في كل من الأحماض والقواعد.
في درجة حرارة الغرفة، يمكن للزئبق أن يتبخر، ويكون كل من بخار الزئبق ومركباته شديد السمية، مما يؤدي إلى آثار صحية مزمنة.
للزئبق تاريخ طويل من الاستخدام ولا يزال يستخدم على نطاق واسع حتى اليوم.

الكادميوم هو عنصر فلزي ثقيل غير حديدي له الرمز الكيميائي Cd والرقم الذري 48. وهو معدن فضي-أبيض يمتلك خصائص ممتازة لامتصاص النيوترونات. وتفيد قضبان الكادميوم في إبطاء معدل التفاعل الانشطاري المتسلسل في المفاعلات النووية. بالإضافة إلى ذلك، يُستخدم في بطاريات الزنك والكادميوم.
يتميز شكل كبريتيد الكادميوم بلون ساطع ويستخدم لإنتاج الصبغة الصفراء المعروفة باسم أصفر الكادميوم.

البزموت عنصر فلزي يمثله الرمز الكيميائي Bi والرقم الذري 83. ينتمي إلى المجموعة VA في الدورة السادسة من الجدول الدوري.
يتميز البزموت بمظهر فريد من نوعه بلونه الأبيض الفضي المائل إلى الوردي، وهو معدن هش يمكن سحقه بسهولة. ويُظهر خواص كيميائية مستقرة نسبياً.
يمكن العثور على البزموت في شكله المعدني الحر وكذلك في معادن مختلفة في الطبيعة.

الذهب (الرمز: Au، العدد الذري: 79) هو عنصر فلزي يُشار إليه غالبًا باسم المعدن الثمين نظرًا لاستخدامه التاريخي كشكل من أشكال العملة ووسيلة لحفظ القيمة وكمجوهرات.
يمكن العثور على الذهب الموجود بشكل طبيعي على شكل شذرات أو حبيبات داخل الصخور والعروق الجوفية والطمي.
وباعتباره أحد المعادن النقدية، يكون الذهب صلباً في درجة حرارة الغرفة ويُعرف بكثافته العالية وليونته وسطوعه ومقاومته للتآكل. وهو ثاني أكثر المعادن قابلية للسحب، بعد البلاتين.

الفضة، التي يُرمز إليها برمزها الكيميائي Ag، هي معدن انتقالي يُستخدم منذ العصور القديمة ويُعتبر معدنًا ثمينًا مهمًا.
على الرغم من إمكانية العثور على الفضة بشكل طبيعي، إلا أنها متوفرة بشكل أساسي في خام الفضة في شكل كيميائي. ويمتاز بخصائص فيزيائية وكيميائية مستقرة إلى حد ما، بما في ذلك التوصيل الحراري والكهربائي الممتاز. ويعكس هذا المعدن الناعم والمرن أكثر من 991 تيرابايت 3 تيرابايت من الضوء، مما يجعله عاكساً للضوء بدرجة عالية. وتحتفظ الفضة بقيمتها كمعدن ثمين نظراً لتعدد استخداماتها الهامة.

البلاتين هو عنصر كيميائي يرمز له بالرمز Pt ويعتبر أحد المعادن الثمينة. ينتمي إلى سلسلة العناصر البلاتينية، ويُشار إليه عادةً باسم "البلاتين". يبلغ وزنه الذري 195.078 ووزنه الذري 78، وهو فلز انتقالي.
تبلغ درجة انصهار البلاتين 1772 درجة مئوية، ودرجة غليانه 3827 درجة مئوية، وكثافته 21.45 جم/سم مكعب عند درجة حرارة 20 درجة مئوية. وهو ناعم نسبياً ويمتلك ليونة جيدة وتوصيل حراري وتوصيل كهربائي جيد.
البلاتين الإسفنجي عبارة عن مادة رمادية اللون تشبه الإسفنج ذات مساحة سطح محددة كبيرة وقدرة امتصاص قوية للغازات، وخاصة الهيدروجين والأكسجين وأول أكسيد الكربون. يمكن أن يمتص البلاتين الأسود المسحوق كمية كبيرة من الهيدروجين.
الروثينيوم هو عنصر فلزي نادر متعدد التكافؤ يُعرف بصلابته وهشاشته ومظهره الرمادي الفاتح. ورمزه الكيميائي Ru وينتمي إلى فلزات المجموعة البلاتينية.
على الرغم من وجوده في القشرة الأرضية، إلا أن الروثينيوم هو أحد أندر المعادن، حيث يبلغ تركيزه واحد في المليار فقط. ويشتهر بخصائصه المستقرة ومقاومته العالية للتآكل.
يتمتع الروثينيوم بالقدرة على تحمل التآكل من حمض الهيدروكلوريك وحمض الكبريتيك وحمض النيتريك والأكوا ريجيا في درجة حرارة الغرفة.
على الرغم من أن الروثينيوم هو أقل معادن مجموعة البلاتين تكلفة، إلا أنه لا يزال أقل وفرة من المعادن الأخرى مثل البلاتين والبلاديوم.

الروديوم هو معدن صلب أبيض فضي اللون يمثله الرمز الكيميائي Rh. وهو ينتمي إلى عناصر مجموعة البلاتين ويُعرف بانعكاسيته العالية.
عادةً، لا يشكل معدن الروديوم أكاسيد، ولكن عندما يكون في حالة منصهرة، يمكنه امتصاص الأكسجين وإطلاقه عند التصلب.
وبالمقارنة مع البلاتين، يتميز الروديوم بدرجة انصهار أعلى وكثافة أقل. وعلاوة على ذلك، فهو غير قابل للذوبان في معظم الأحماض وغير قابل للذوبان تمامًا في حمض النيتريك. وهو قابل للذوبان بشكل طفيف فقط في أكوا ريجيا.
البلاديوم هو فلز انتقالي ينتمي إلى مجموعة البلاتين، ورمزه الكيميائي Pd. يقع في المجموعة الثامنة من الدورة الخامسة من الجدول الدوري.
والبلاديوم في شكله النقي هو معدن أبيض فضي له ملمس ناعم وليونة وليونة جيدة. وهذا يجعل من السهل تشكيله ولفه وسحبه إلى أشكال مختلفة.
ويتميز البلاديوم بخاصية فريدة من نوعها تتمثل في قدرته على امتصاص غاز الهيدروجين، مما يؤدي إلى زيادة كبيرة في الحجم. ومع ذلك، يمكن أن تتسبب هذه الخاصية أيضًا في أن يصبح المعدن هشًا وحتى يتكسر إلى شظايا.

الأوزميوم عنصر كيميائي يرمز له الرمز Os والعدد الذري 76. ينتمي إلى المجموعة الثامنة في الدورة السادسة من الجدول الدوري، وتبلغ كتلته الذرية النسبية 190.23.
وباعتباره عضوًا في مجموعة البلاتينيوم، يُعد الأوزميوم فلزًا ثقيلًا ذا أعلى كثافة بين جميع العناصر.

الإيريديوم هو عنصر فلزي رمزه الكيميائي Ir ورقمه الذري 77. وزنه الذري 192.22، واسمه مشتق من الكلمة اللاتينية التي تعني "قوس قزح".
يندر وجود الإيريديوم في القشرة الأرضية، حيث يوجد بتركيز 1/10 مليون فقط. وعادةً ما يكون منتشراً في خامات مختلفة ويمكن العثور عليه في الرواسب الغرينية والرملية، إلى جانب عناصر أخرى في سلسلة البلاتين.
البريليوم هو عنصر كيميائي يُمثِّله الرمز Be وعدده الذري 4. يُصنَّف ضمن المجموعة الرئيسية الثانية والدورة الثانية من الجدول الدوري.
ينتمي هذا المعدن القلوي الترابي القلوي الأبيض المائل للرمادي إلى النظام السداسي ويعرف بصلابته وانخفاض معامل التمدد الحراري. ومع ذلك، يجب التعامل معه بحذر لأن البريليوم ومركباته شديدة السمية.
البريليوم معدن مذبذب ويمكن أن يذوب في كل من الأحماض والقواعد. وتتنوع تطبيقاته، بدءاً من استخدامه كمادة في مفاعلات الطاقة الذرية وهندسة الطيران إلى دمجه في سبائك مختلفة وكمكون في نوافذ الإرسال بالأشعة السينية.

الليثيوم هو عنصر فلزي يرمز له بالرمز الكيميائي Li وله مظهر أبيض فضي ناعم. وهو الأقل كثافة بين جميع الفلزات.
يُستخدم الليثيوم في تطبيقات مختلفة، بما في ذلك المفاعلات الذرية والسبائك الخفيفة والبطاريات. وخلافاً للفلزات القلوية الأخرى، يتمتع الليثيوم ومركباته بخصائص غير نمطية بسبب كثافة شحنته العالية وطبقة الإلكترونات المزدوجة المستقرة من نوع الهيليوم. وبالتالي، يسهل استقطابها بسهولة بواسطة جزيئات أو أيونات أخرى ولكن يصعب استقطابها بنفسها.
تؤثر هذه الخاصية الفريدة على ثبات الليثيوم ومركباته. ويتمتع الليثيوم بأكثر إمكانات القطب الكهربائي سالبة بين جميع العناصر المعروفة، بما في ذلك العناصر المشعة، وهو ما يجعله أكثر الفلزات تفاعلية.

الروبيديوم هو فلز أبيض فضي فاتح اللون يُرمز له بالرمز الكيميائي Rb. ويتميز بقوامه الناعم والشمعي ويعرض خواص كيميائية أكثر نشاطاً من البوتاسيوم.
من المعروف أن الروبيديوم يبعث إلكترونات عند تعرضه للضوء. ويتفاعل بقوة مع الماء، منتجاً هيدروكسيد الروبيديوم والهيدروجين. بالإضافة إلى ذلك، يتفاعل بسهولة مع الأكسجين لتكوين أكاسيد معقدة.
ونظراً للحرارة الكبيرة المتولدة أثناء التفاعل مع الماء، هناك خطر اشتعال الهيدروجين على الفور. وكإجراء احترازي، يتم تخزين معدن الروبيديوم النقي عادةً في عبوات زجاجية محكمة الغلق لمنع ملامسته للهواء أو الرطوبة.

السيزيوم عنصر في الجدول الدوري ورمزه Cs ورقمه الذري 55. يُصنَّف كعنصر من عناصر المجموعة IA في الدورة السادسة.
السيزيوم في شكله العنصري هو معدن أصفر ذهبي فاتح تفاعلي ذو درجة انصهار منخفضة. وهو شديد الحساسية للهواء وعرضة للأكسدة.
عندما يتلامس السيزيوم مع الماء، فإنه يتفاعل بعنف وقد ينفجر منتجاً الهيدروجين. لا يوجد السيزيوم في الطبيعة إلا في صورة ملح ونادراً ما يوجد في البر والبحر.
السيزيوم مادة مهمة في إنتاج أجهزة التفريغ والخلايا الضوئية. وكان النظير المشع Cs-137 من بين الملوثات التي تسربت من محطة فوكوشيما داييشي للطاقة النووية في اليابان.
السيزيوم هو الأكثر فلزية بين جميع العناصر المعروفة، بما في ذلك العناصر المشعة. وتجدر الإشارة إلى أن الليثيوم هو أكثر العناصر تفاعلية.

تيتانيوم هو عنصر كيميائي يرمز له الرمز Ti والرقم الذري 22. ينتمي إلى المجموعة IVB في الدورة الرابعة من الجدول الدوري وهو فلز انتقالي أبيض فضي اللون معروف بخفة وزنه وقوته العالية وبريقه المعدني ومقاومته للتآكل بفعل الكلور الرطب.
ومع ذلك، فإن التعرض للكلور الجاف يمكن أن يسبب تفاعلاً كيميائياً عنيفاً في التيتانيوم، حتى في درجات حرارة أقل من 0 درجة مئوية. وينتج هذا التفاعل رابع كلوريد التيتانيوم ويتحلل لينتج ثنائي كلوريد التيتانيوم، الذي يمكن أن يشتعل في الحالات القصوى. ولذلك، لا يمكن أن يظل التيتانيوم مستقراً إلا عندما يكون محتوى الماء في الكلور أعلى من 0.51 ت ف 3 ت.
يُعتبر التيتانيوم معدنًا نادرًا نظرًا لتواجده المتناثر في الطبيعة وصعوبة استخراجه. وعلى الرغم من ذلك، فهو وفير نسبياً ويحتل المرتبة العاشرة بين جميع العناصر. وتوجد خامات التيتانيوم الرئيسية، وهي الإلمنيت والروتيل، على نطاق واسع في القشرة الأرضية والغلاف الصخري. بالإضافة إلى ذلك، يمكن العثور على التيتانيوم في جميع الكائنات الحية والصخور والمياه والتربة تقريباً.

الزركونيوم عنصر كيميائي يرمز له الرمز Zr والرقم الذري 40. وهو معدن رمادي فاتح ذو درجة انصهار عالية.
عند تعريض سطح الزركونيوم للهواء، يطور سطح الزركونيوم بسرعة طبقة أكسيد تمنحه مظهراً لامعاً يشبه الفولاذ. كما أنه يتمتع بمقاومة فائقة للتآكل، وهو قابل للذوبان في كل من حمض الهيدروفلوريك وحمض أكوا ريجيا.
يمكن أن يتفاعل الزركونيوم مع كل من غير معدنية والعناصر الفلزية عند درجات حرارة عالية، مكونةً محاليل صلبة.

الفاناديوم هو عنصر فلزي يرمز له بالرمز V. وهو فلز رمادي فضي ينتمي إلى المجموعة 5 في الجدول الدوري للعناصر. العدد الذري للفاناديوم 23 والوزن الذري 50.9414. وهو ذو بنية بلورية مكعبة متمركزة على الجسم وله تكافؤات شائعة +5 و+4 و+3 و+2.
يُصنف الفاناديوم كمعدن حراري بسبب درجة انصهاره العالية. بالإضافة إلى ذلك، فهو مطيل وصلب وغير مغناطيسي. كما يتميز الفاناديوم أيضاً بمقاومة عالية لحمض الهيدروكلوريك وحمض الكبريتيك، كما أنه يُظهر مقاومة أفضل للتآكل من الغازات والأملاح والماء مقارنةً بمعظم أنواع الفولاذ المقاوم للصدأ.

النيوبيوم هو عنصر فلز انتقالي رمزه الكيميائي Nb ورقمه الذري 41. وهو فلز رمادي لامع.
في شكله النقي، يكون النيوبيوم في شكله النقي مطيلًا للغاية. ومع ذلك، تزداد صلابته مع زيادة محتوى الشوائب. وبالإضافة إلى ذلك، يتميز النيوبيوم بمقطع عرضي منخفض للغاية لالتقاط النيوترونات الحرارية، مما يجعله ذا قيمة عالية في الصناعة النووية.

التنتالوم عنصر فلزي عدده الذري 73 ورمزه الكيميائي Ta. وشكله العنصري عبارة عن معدن رمادي-فولاذي يُظهر مقاومة عالية للتآكل.
لا يُظهر التنتالوم أي تفاعلية تجاه حمض الهيدروكلوريك أو حمض النيتريك المركز أو أكوا ريجيا في كل من الظروف الباردة والساخنة. ويوجد في المقام الأول في التنتاليت، وغالباً ما يتعايش مع النيوبيوم.
يُظهر التنتالوم صلابة وليونة معتدلة ويمكن سحبه إلى سلك رفيع أو رقائق معدنية. ويتميز بمعامل تمدد حراري صغير وخصائص كيميائية ممتازة ومقاومة عالية للتآكل.
يُستخدم التنتالوم في إنتاج أوعية التبخير وكقطب كهربائي ومقوِّم ومكثف إلكتروليتي في الأنابيب الإلكترونية. وفي الطب، يُستخدم في صناعة صفائح أو خيوط رقيقة لإصلاح الأنسجة التالفة.
ترجع المقاومة القوية للتآكل في التنتالوم إلى تكوين طبقة واقية مستقرة من خامس أكسيد التنتالوم (Ta2O5) على سطحه.

التنجستن هو عنصر فلزي رمزه الكيميائي W ورقمه الذري 74. ينتمي إلى مجموعة VIB من الدورة السادسة في الجدول الدوري للعناصر.
وفي الطبيعة، يوجد التنغستن في المقام الأول في شكل كاتيونات سداسية التكافؤ، التي يبلغ نصف قطر أيونها 0.68 × 10^10-10 متر. ونظرًا لصغر نصف قطر أيون التنغستن وقدرته الكهربية العالية وقدرته القوية على الاستقطاب، فإنه يشكل بسهولة أنيونات معقدة. وهكذا، غالبًا ما يظهر التنجستن في شكل أنيونات معقدة، مثل [WO4]^2- في رواسب الولفراميت أو الشكيليت.
يظهر التنجستن في شكله العنصري كمعدن أبيض فضي لامع ذو صلابة عالية ودرجة انصهار عالية. وهو مقاوم للتآكل بفعل الهواء في درجة حرارة الغرفة ويمتلك خواص كيميائية مستقرة نسبياً. ويستخدم التنغستن في العديد من التطبيقات، بما في ذلك تصنيع الخيوط وسبائك القطع عالية السرعة والقوالب فائقة الصلابة والأدوات البصرية والكيميائية. وتمتلك الصين أكبر احتياطي من التنغستن في العالم.

الموليبدينوم هو عنصر كيميائي يحمل الرمز Mo والرقم الذري 42. وهو ينتمي إلى مجموعة المعادن الانتقالية، وهو عنصر مهم للغاية لصحة الإنسان، ويوجد في أنسجة مختلفة من الجسم مثل الكبد والكلى.
يحتوي جسم الإنسان على حوالي 9 ملغ من الموليبدينوم إجمالاً. ويُعرف هذا المعدن الأبيض الفضي بصلابته وقوته، وهو مهم لنمو النباتات والحيوانات على حد سواء.

الغاليوم هو عنصر فلزي يظهر بلون أزرق مائل للرمادي أو أبيض مائل للفضي، ويمثله الرمز الكيميائي Ga ووزنه الذري 69.723.
على الرغم من وجود درجة انصهار منخفضة، فإن الغاليوم لديه درجة غليان عالية. عندما يكون الغاليوم في شكله السائل النقي، فإنه يميل إلى التبريد الفائق ويتأكسد بسهولة في الهواء، مما يؤدي إلى تكوين طبقة أكسيد.

الإنديوم عنصر فلزي رمزه "إن" وعدده الذري 49. ينتمي إلى المجموعة IIIA في الدورة الخامسة من الجدول الدوري.
يظهر الإنديوم في حالته النقية على هيئة معدن أبيض فضي مع لون أزرق فاتح. وهو ناعم للغاية ويمكن خدشه بسهولة باستخدام ظفر الإصبع. وعلاوة على ذلك، يُظهر الإنديوم قابلية ملحوظة للطرق والليونة مما يتيح تشكيله في أشكال مختلفة.
يُستخدم الإنديوم بشكل أساسي كمادة أساسية في تصنيع السبائك ذات درجة الانصهار المنخفضة والسبائك الحاملة وأشباه الموصلات ومصادر الضوء الكهربائي.

الثاليوم، الذي يرمز له بالرمز Tl والعدد الذري 81، هو عنصر من المجموعة IIIA ينتمي إلى الدورة السادسة من الجدول الدوري.
ونظراً لكونه عنصراً نادراً، فإنه يوجد بكميات قليلة في البيئة الطبيعية. ويذوب الثاليوم ببطء في حمض الهيدروكلوريك وحمض الكبريتيك المخفف، لكنه يذوب بسرعة في حمض النيتريك.
تشمل المركبات الأساسية للثاليوم الأكاسيد والكبريتيدات والهاليدات والكبريتات. أملاح الثاليوم عبارة عن بلورات عديمة اللون وعديمة الطعم تذوب في الماء مكونة مركبات الثاليوم.
الثاليوم أكثر استقرارًا نسبيًا في الماء أو البارافين مقارنةً بالهواء.

الجرمانيوم هو عنصر كيميائي يرمز له بالرمز Ge والرقم الذري 32 والوزن الذري 72.64. يقع في الدورة الرابعة والمجموعة IVA من الجدول الدوري للعناصر.
الجرمانيوم معدن لامع وصلب وأبيض مائل للرمادي. وهو ينتمي إلى مجموعة الكربون، وتتشابه خواصه الكيميائية مع خواص القصدير والسيليكون، وهما أيضاً من نفس المجموعة.
الجرمانيوم غير قابل للذوبان في الماء وحمض الهيدروكلوريك والمحاليل الكاوية المخففة، ولكنه قابل للذوبان في أكوا ريجيا أو حمض النيتريك المركز أو حمض الكبريتيك. له خواص مذبذبة وهو قابل للذوبان في القلويات المنصهرة أو القلويات البيروكسيدية أو نترات الفلزات القلوية أو الكربونات. وهو مستقر نسبياً في الهواء.
توجد خمسة نظائر مستقرة للجرمانيوم في الطبيعة: 70Ge و72Ge و73Ge و74Ge و76Ge. عندما يتفاعل الجرمانيوم مع الأكسجين فوق 700 درجة مئوية، فإنه يشكل GeO2. وعندما يتفاعل مع الهيدروجين فوق 1000 درجة مئوية، يمكن أن يشتعل في الكلور أو البروم.
الجرمانيوم هو شبه موصل ممتاز ويمكن استخدامه للكشف عن التيارات عالية التردد وتقويم التيار المتردد. كما يمكن استخدامه كمادة ضوئية تعمل بالأشعة تحت الحمراء وفي الأدوات الدقيقة وكمحفز. يمكن استخدام مركبات الجرمانيوم في صناعة ألواح الفلورسنت والنظارات المختلفة ذات معامل الانكسار العالي.

الرينيوم هو عنصر كيميائي يُرمز له بالرمز Re وعدده الذري 75. وهو فلز كثيف أبيض فضي اللون ينتمي إلى الدورة السادسة للفلزات الانتقالية في الجدول الدوري للعناصر.
الرينيوم عنصر نادر للغاية يوجد في القشرة الأرضية بمتوسط تركيز يقدر بمليار واحد فقط. وهو معروف أيضاً بأنه من أعلى درجات الانصهار والغليان بين جميع العناصر.
تنتج عملية تكرير الموليبدينوم والنحاس الرينيوم كمنتج ثانوي. وللرينيوم خواص كيميائية مماثلة للمنجنيز والتكنيتيوم.
تحتوي مركبات الرينيوم على حالات أكسدة تتراوح بين -3 و+7، حيث إن -3 هي الأقل و+7 هي الأعلى.

اللانثانوم عنصر فلزي ترابي نادر رمزه الكيميائي La، وعدده الذري 57، ووزنه الذري 138.90547. يأتي اسم هذا العنصر من اللغة اليونانية ويعني في الأصل "الكامن في الخفاء".
يتميز اللانثانوم ببريق رمادي فضي وملمس ناعم، وتبلغ كثافته 6.162 جم/سم3. وتبلغ درجة انصهاره 920 درجة مئوية، ودرجة غليانه 3464 درجة مئوية عند الضغط الجوي. يُظهر خواص كيميائية نشطة ويفقد بريقه المعدني بسرعة عند تعرضه للهواء، مكونًا طبقة من طبقة من الأكسيد الأزرق. ومع ذلك، فإن هذا الفيلم غير قادر على حماية المعدن، مما يؤدي إلى استمرار الأكسدة وتكوين مسحوق أكسيد أبيض.
يتفاعل اللانثانوم ببطء مع الماء البارد، وهو قابل للذوبان في الأحماض، ويمكن أن يتفاعل مع مختلف اللافلزات. عادةً ما يتم تخزين المعدن في زيت معدني أو غاز نادر.
وتحتوي القشرة الأرضية على 0.001831 تيرابايت 3 تيرابايت من اللانثانوم، مما يجعله ثاني أكثر العناصر الأرضية النادرة وفرة بعد السيريوم. يوجد نظيران طبيعيان لللانثانوم: اللانثانوم-139 واللانثانوم-138 المشع.

السيريوم عنصر ترابي نادر عدده الذري 58. وهو ينتمي إلى مجموعة اللانثانيدات IIIB في الدورة السادسة من الجدول الدوري ويمثله الرمز الكيميائي Ce. يظهر في شكله العنصري على هيئة فلز تفاعلي رمادي فضي اللون.
تجدر الإشارة إلى أن السيريوم عرضة للاحتراق التلقائي عندما يكون في شكل مسحوق ويمكن أن يذوب في الأحماض والعوامل المختزلة.

البراسيوديميوم فلز ترابي نادر عدده الذري 59. يعود أصل اسمه إلى اللغة اليونانية، ويعني "الأخضر". للبراسيوديميوم بنية بلورية سداسية الشكل.
بالمقارنة مع اللانثانوم والسيريوم والنيوديميوم واليوروبيوم، يُظهر البراسيوديميوم مقاومة أكبر للتآكل في الهواء. ومع ذلك، عند تعرضه للهواء، فإنه لا يزال يشكل طبقة من الأكسيد الأخضر الهش. يجب تخزين البراسيوديميوم النقي في زيت معدني أو حاوية بلاستيكية محكمة الغلق.
يُستخدم البراسيوديميوم في التكسير التحفيزي للبترول. يمكن أن تؤدي إضافة إثراء البراسيوديميوم والنيوديميوم المخصب إلى المنخل الجزيئي Y-زيوليت إلى تعزيز نشاط وانتقائية واستقرار محفز التكسير البترولي.
على غرار العناصر الأرضية النادرة الأخرى، يتميز البراسيوديميوم بسمية منخفضة وليس ضروريًا للعمليات البيولوجية.

ينتمي النيوديميوم، الذي يرمز له بالرمز Nd وعدده الذري 60، إلى سلسلة العناصر اللانثانيدية. وهو فلز أبيض فضي اللون وأحد أكثر المعادن الأرضية النادرة تفاعلية.
تبلغ كثافة النيوديميوم 7.004 جم/سم مكعب ودرجة انصهاره 1024 درجة مئوية. وهو أيضاً بارامغناطيسي بارامغناطيسي وسرعان ما يغمق لونه عند تعرضه للهواء، مكوناً أكاسيد. ويتفاعل ببطء مع الماء البارد وبسرعة مع الماء الساخن.
يمكن أن يحل زجاج النيوديميوم المطعّم بالإيتريوم الإيتريوم الألومنيوم وزجاج النيوديميوم محل الياقوت كمواد ليزر، بينما يمكن استخدام زجاج النيوديميوم والبراسيوديميوم كنظارات واقية.
يُعد النيوديميوم عنصراً أساسياً في صناعة التربة النادرة ويلعب دوراً هاماً في تنظيم سوق التربة النادرة.

السماريوم هو عنصر فلزي رمزه الكيميائي Sm وعدده الذري 62. لونه أبيض مائل للفضة، وصلابته متوسطة، وهو عرضة للأكسدة عند تعرضه للهواء.
وباعتباره ممثلًا لسلسلة اللانثانيد، يوجد السماريوم عادةً في حالة أكسدة +3. تشمل مركبات السماريوم الأكثر انتشارًا SmO وSMS وSMI2 وSMTe.
لا يُعرف أن للساماريوم أي تأثيرات بيولوجية كبيرة ولا يُظهر سوى سمية طفيفة.

اليوروبيوم عنصر فلزي ذو لون أبيض فضي يمكن أن يتأكسد إلى أكسيد أبيض تقريباً. وتبلغ درجة انصهاره 822 درجة مئوية، ودرجة غليانه 1597 درجة مئوية، وكثافته 5.2434 جم/سم مكعب.
ومن بين العناصر الأرضية النادرة، يُعد اليوروبيوم أنعم العناصر الأرضية النادرة وأكثرها تطايراً وهو أيضاً أكثر المعادن تفاعلاً. وعند تعريضه للهواء في درجة حرارة الغرفة، يفقد بريقه المعدني ويتأكسد بسرعة ليتحول إلى مسحوق.
يتفاعل اليوروبيوم بعنف مع الماء البارد، وينتج الهيدروجين. بالإضافة إلى ذلك، يمكن أن يتفاعل مع البورون والكربون والكبريت والفوسفور والهيدروجين والنيتروجين.
لليوروبيوم العديد من التطبيقات العملية. فهو يُستخدم على نطاق واسع في إنتاج مواد التحكم في المفاعلات ومواد الحماية من النيوترونات، وكذلك في صناعة الطاقة الذرية كفوسفور للتلفزيون الملون وفي إنتاج مواد الليزر من اليوروبيوم (Eu).
اليوروبيوم هو أحد أندر العناصر الأرضية النادرة على الأرض، حيث يبلغ محتواه 1.1 جزء في المليون فقط. وهو معدن ناعم ولامع ورمادي مائل إلى الفولاذ مع ليونة قوية وقابلية للطرق، مما يجعله سهل المعالجة في أشكال مختلفة. وهو يشبه الرصاص في المظهر والملمس ولكنه أثقل قليلاً.

الجادولينيوم هو عنصر فلزي يرمز له بالرمز Gd، ويبلغ عدده الذري 64 ووزنه الذري 157.25. ويتميز بمظهر أبيض فضي اللون وهو مطيل بطبيعته. سُمِّيَ هذا العنصر على اسم العالم الفنلندي جادولين، الذي قدم إسهامات كبيرة في دراسة اللانثانيدات.
عُزِل الجادولينيوم لأول مرة في مالايا بسويسرا عام 1880، وحضّر شكله النقي وسماه الكيميائي الفرنسي بوفابودراند عام 1886. ويوجد في المقام الأول في معادن مثل المونازيت والباستنازيت، وتبلغ وفرة هذا المعدن في القشرة الأرضية 0.000636% فقط.
يحتوي الجادولينيوم على مجموعة واسعة من التطبيقات في مجالات مثل الطب والصناعة والتكنولوجيا النووية وغيرها.

التيربيوم هو عضو في سلسلة اللانثانيد ويمثله الرمز الكيميائي Tb وعدده الذري 65. يقع في المجموعة الثالثة من الدورة السادسة للجدول الدوري وله مظهر معدني فضي-أبيض في شكله العنصري.
ونظراً لكونه فلزاً ترابياً نادراً، فإن التيربيوم سام وله نظير واحد مستقر فقط يوجد بشكل طبيعي، إلى جانب 20 نظيراً مشعاً إضافياً. ويمتلك بنية بلورية سداسية الشكل ويذوب في حمض مخفف، ولكنه يتفاعل ببطء مع الماء.
نظرًا لتفاعليته العالية، يجب تخزين التيربيوم في حاوية مملوءة بغاز خامل أو حاوية مفرغة من الهواء.
الديسبروسيوم هو فلز أبيض فضي ناعم ناعم يرمز له بالرمز الكيميائي Dy. وتبلغ درجة انصهاره 1412 درجة مئوية، ودرجة غليانه 2562 درجة مئوية، وكثافته 8.55 جم/سم مكعب. حتى أنه قادر على إظهار الموصلية الفائقة بالقرب من الصفر المطلق.
على الرغم من أن الديسبروسيوم مستقر نسبيًا عند تعرضه للهواء، إلا أنه يمكن أن يتأكسد بسهولة عن طريق الهواء والماء في درجات حرارة عالية، مما يؤدي إلى تكوين أكسيد الديسبروسيوم.
ويجد الديسبروسيوم تطبيقات واسعة النطاق في مجالات مختلفة، بما في ذلك تصنيع مصادر الإضاءة الجديدة مثل مصابيح الديسبروسيوم، كمادة تحكم في المفاعلات، وكمحفز في صناعة تكرير النفط في شكل مركبات الديسبروسيوم.

الهولميوم هو عنصر فلزي رمزه الكيميائي هو، ووزنه الذري 67، ووزنه الذري 164.93. وقد سُمي بهذا الاسم نسبة إلى مسقط رأس مكتشفه في ستوكهولم، الذي حدده لأول مرة من طيف الإربيوم الترابي في عام 1878. وفي العام التالي، فصل كلايف السويدي الهولميوم عن الإربيوم الترابي باستخدام طرق كيميائية.
يبلغ تركيز الهولميوم في القشرة الأرضية 0.000115%، ويوجد في المونازيت والخامات الأرضية النادرة، إلى جانب عناصر أرضية نادرة أخرى. والهولميوم-165 هو النظير الوحيد المستقر للهولميوم. وهو معدن أبيض مائل للفضة، وهو معدن ناعم وقابل للسحب، وتبلغ درجة انصهاره 1474 درجة مئوية، ودرجة غليانه 2695 درجة مئوية، وكثافته 8.7947 جم/سم مكعب.
على الرغم من أن الهولميوم مستقر في الهواء الجاف، إلا أنه يتأكسد بسرعة في درجات الحرارة العالية. وأكسيد الهولميوم هو أكثر المواد البارامغناطيسية المعروفة، ويمكن استخدام مركبات الهولميوم كمواد مضافة للمواد المغناطيسية الحديدية الجديدة. ويستخدم يوديد الهولميوم في صناعة مصابيح الهاليد المعدنية، مثل مصابيح الهولميوم، ويستخدم ليزر الهولميوم على نطاق واسع في المجال الطبي.

الإربيوم هو عنصر موجود في الجدول الدوري ورمزه Er وعدده الذري 68. وهو ينتمي إلى سلسلة اللانثانيدات ويقع في المجموعة الثالثة ب من الدورة السادسة، ويبلغ وزنه الذري 167.26. يأتي اسم العنصر من موقع اكتشافه، وهو الإيتريوم الأرضي.
اكتشف العالم السويدي موساندر أول مرة أكسيد الإربيوم في التراب الإيتريوم في عام 1843، وسُمي رسمياً في عام 1860. ويبلغ محتوى الإربيوم في القشرة الأرضية 0.000247%، وهو موجود في العديد من المعادن الأرضية النادرة. وتوجد ستة نظائر طبيعية للإربيوم، وهي 162 و164 و166 و167 و168 و170.

الثوليوم هو معدن أبيض فضي ناعم ناصع البياض يرمز له بالرمز الكيميائي TM. وهو قابل للطرق ويمكن قطعه بسهولة بالسكين. تبلغ درجة انصهار الثوليوم 1545 درجة مئوية ودرجة غليانه 1947 درجة مئوية وكثافته 9.3208.
وهو مستقر نسبيًّا في الهواء، ويظهر شكل أكسيده على هيئة بلورة خضراء فاتحة. العدد الذري للثوليوم 69 والوزن الذري 168.93421. اسم العنصر مشتق من البلد الذي اكتُشف فيه.
والثوليوم هو أقل العناصر الأرضية النادرة وفرة، حيث يبلغ تركيزه في القشرة الأرضية جزأين فقط لكل 100,000. ويوجد في المقام الأول في خامات الإيتريوم والفوسفور والمناجم الأرضية النادرة السوداء. والنظير الطبيعي الوحيد المستقر للثوليوم هو 169.
للثوليوم تطبيقات مختلفة في مجالات مختلفة، بما في ذلك مصادر الضوء عالية الكثافة لتوليد الطاقة والليزر والموصلات الفائقة عالية الحرارة وغيرها.

الإيتربيوم هو عنصر فلزي رمزه الكيميائي Yb، وعدده الذري 70، ووزنه الذري 173.04. واسمه مشتق من المكان الذي اكتُشف فيه.
يبلغ تركيز الإيتربيوم في القشرة الأرضية 0.000266%. ويوجد في المقام الأول في خامات الإيتريوم والفوسفور والمناجم الأرضية النادرة السوداء. توجد سبعة نظائر طبيعية للإيتربيوم.
اللوتيتيوم هو عنصر فلزي يرمز له بالرمز الكيميائي Lu. وهو معدن فضي-أبيض، وهو أقسى العناصر الأرضية النادرة وأكثفها، حيث تبلغ درجة انصهاره 1663 درجة مئوية، ودرجة غليانه 3395 درجة مئوية، وكثافته 9.8404. اللوتيتيوم مستقر نسبياً في الهواء، وشكل أكسيده عبارة عن بلورة عديمة اللون تذوب في الحمض لتكوين ملح عديم اللون مطابق.
على الرغم من أن اللوتيتيوم له احتياطيات طبيعية محدودة، إلا أن له العديد من الاستخدامات، خاصة لأغراض البحث. وهو قابل للذوبان في الأحماض المخففة ويتفاعل ببطء مع الماء. أملاحه عديمة اللون، وأكاسيده بيضاء اللون. نظيرا اللوتيتيوم الموجودان بشكل طبيعي هما 175 لو، وعمره النصفي 2.1 × 10 × 1010 سنوات، و 176 لـو
وبسبب احتياطياته الطبيعية المحدودة، يُعد اللوتيتيوم عنصرًا باهظ الثمن.

السكانديوم هو عنصر كيميائي يرمز له الرمز Sc والرقم الذري 21. وهو فلز انتقالي ناعم أبيض فضي اللون، ويُخلط أحيانًا مع الجادولينيوم والإربيوم.
إن إنتاج السكانديوم محدود للغاية، ويبلغ تركيزه في القشرة الأرضية حوالي 0.00051 تيرابايت 3 تيرابايت. ويُستخدم عادة في إنتاج الزجاج المتخصص والسبائك خفيفة الوزن والمقاومة للحرارة.

الإيتريوم هو معدن أسود مائل إلى الرمادي يُعرف بالرمز الكيميائي Y. ويُعتبر أول عنصر فلز أرضي نادر تم اكتشافه وهو معروف بقابليته للسحب. يتفاعل الإيتريوم بسهولة مع الماء الساخن ويمكن إذابته في الأحماض المخففة. بالإضافة إلى ذلك، يُستخدم في إنتاج زجاج وسبائك خاصة.

الثوريوم هو عنصر فلزي مشع يُعرف بالرمز الكيميائي Th. وتكمن إمكانياته كوقود نووي في قدرته على التحول إلى يورانيوم-233 عند تعرضه لقصف نيوتروني. ويتميز الثوريوم بملمس ناعم وبريق رمادي ويتميز بخصائصه الكيميائية النشطة. وهو منتشر على نطاق واسع في جميع أنحاء القشرة الأرضية ويعتبر مادة واعدة في مجال الطاقة لتطبيقاته المحتملة في مجال الطاقة النووية.

الهفنيوم هو عنصر فلزي رمزه الكيميائي Hf، ووزنه الذري 72، ووزنه الذري 178.49. يظهر في شكل فلز انتقالي لامع لونه فضي-رمادي في شكله النقي. وتوجد ستة نظائر مستقرة للهافنيوم في الطبيعة: الهافنيوم-174 والهافنيوم-176 والهافنيوم-177 والهافنيوم-178 والهافنيوم-179 والهافنيوم-180.
الهافنيوم غير تفاعلي نسبيًا ولا يتفاعل مع حمض الهيدروكلوريك المخفف أو حمض الكبريتيك المخفف أو المحاليل القلوية القوية. ومع ذلك، فهو قابل للذوبان في حمض الهيدروفلوريك وحمض الهيدروفلوريك والماء الملكي. وتركيز الهافنيوم في القشرة الأرضية منخفض نسبيًا، حيث يبلغ 0.000451 تيرابايت 3 تيرابايت فقط. وغالباً ما يوجد مع الزركونيوم في الطبيعة.

السيليكون، المعروف أيضاً باسمه السابق السيليسيوم، هو عنصر كيميائي يُرمز له بالرمز Si. يبلغ عدده الذري 14 والكتلة الذرية النسبية 28.0855، ويوجد في شكلين: السيليكون غير المتبلور والبلوري.
في الجدول الدوري، يقع السيليكون في الدورة الثالثة ويصنف كعنصر فلزي في المجموعة IVA. وهو عنصر عالي الوفرة، ويحتل المرتبة الثامنة في الكون.
على الرغم من وفرة السيليكون النقي إلا أنه نادر في الطبيعة. ويوجد عادة في السيليكات المعقدة أو السيليكا الموجودة في الصخور والحصى والغبار.
السيليكون هو ثاني أكثر العناصر وفرة في القشرة الأرضية، حيث يمثل 26.41 تيرابايت 3 تيرابايت من الكتلة الكلية. أما الأكسجين فهو العنصر الأكثر وفرة حيث يشكل 49.41 تيرابايت 3 تيرابايت من القشرة الأرضية.

السيلينيوم هو غير معدنية عنصر يمثله الرمز الكيميائي Se. يقع في المجموعة السادسة أ من الدورة الرابعة في الجدول الدوري للعناصر (العنصر 34). للسيلينيوم العديد من التطبيقات، بما في ذلك العمل كمادة حساسة للضوء، ومحفز في صناعة المنجنيز الإلكتروليتي، ومغذٍ أساسي للحيوانات، بالإضافة إلى كونه مغذٍ مفيد للنباتات.
ويوجد السيلينيوم في الطبيعة في شكلين: السيلينيوم غير العضوي والسيلينيوم النشط نباتياً. ويتكون السيلينيوم غير العضوي من سيلينيت الصوديوم وسيلينات الصوديوم، اللذان يتم الحصول عليهما من المنتجات الثانوية لرواسب المعادن.
من ناحية أخرى، ينتج السيلينيوم النشط نباتيًا من مزيج من السيلينيوم والأحماض الأمينية من خلال التحول الحيوي. وغالبًا ما يكون موجودًا في شكل سيلينوميثيونين.

السيلينيوم عنصر غير فلزي يمثله الرمز الكيميائي Se. وهو ينتمي إلى المجموعة السادسة أ من الجدول الدوري للعناصر ويقع في الدورة الرابعة كعنصر 34. للسيلينيوم استخدامات متعددة، بما في ذلك استخدامه كمادة حساسة للضوء، ومحفز في صناعة المنجنيز الإلكتروليتي، وكمغذٍ حيوي للحيوانات ومغذٍ مفيد للنباتات.
ويوجد السيلينيوم في الطبيعة في شكلين: السيلينيوم غير العضوي والسيلينيوم النشط نباتياً. يتم الحصول على السيلينيوم غير العضوي كمنتج ثانوي من الرواسب المعدنية ويشمل سيلينيت الصوديوم وسيلينات الصوديوم.
من ناحية أخرى، يتم إنتاج السيلينيوم النشط نباتيًا من خلال التحول الحيوي عن طريق الجمع بين السيلينيوم والأحماض الأمينية. ويوجد عادةً في شكل سيلينوميثيونين.

الزرنيخ، المعروف أيضًا باسم As، هو عنصر غير فلزي يوجد في المجموعة VA من الدورة الرابعة في الجدول الدوري للعناصر. عدده الذري 33 ويوجد في ثلاثة أشكال متآصلة مختلفة: الزرنيخ الرمادي والأسود والأصفر.
ينتشر هذا العنصر على نطاق واسع في الطبيعة، وقد تم اكتشاف العديد من المعادن المحتوية على الزرنيخ. يُستخدم الزرنيخ ومركباته لأغراض مختلفة، بما في ذلك في المبيدات الحشرية ومبيدات الأعشاب والمبيدات الحشرية والسبائك. ومع ذلك، فإن مركبه ثالث أكسيد الزرنيخ شديد السمية.

البورون، الذي يرمز له بالرمز B، هو عنصر كيميائي موجود في القشرة الأرضية بتركيز 0.0011 تيرابايت 3 تيرابايت فقط. ويوجد عادةً في شكل مواد صلبة سوداء أو رمادية فضية رمادية ذات بنية بلورية سوداء، وله صلابة لا تلي الماس إلا في الصلابة ولكنه هش في الملمس.
ما يميز البورون عن العناصر الأخرى هو رقم التنسيق المرتفع بشكل غير عادي في هيدريده، وهو نتيجة لنقص الإلكترونات. ونتيجة لذلك، فإنه يحتوي على أكثر الهيدريدات العنصرية تعقيدًا.

الراديوم، الذي يرمز له بالرمز Ra، هو عنصر عالي الإشعاع ينتمي إلى الدورة السابعة، المجموعة IIA، ويبلغ عدده الذري 88 في الجدول الدوري للعناصر.
على الرغم من أن معدن الراديوم النقي عديم اللون تقريبًا، فإنه يتفاعل مع النيتروجين في الهواء لتكوين نيتريد الراديوم الأسود (Ra3N2).
وتُظهِر جميع نظائر الراديوم نشاطاً إشعاعياً قوياً، حيث إن الراديوم-226 هو النظير الأكثر استقراراً. ويبلغ نصف عمره 1600 سنة تقريباً ويضمحل إلى الراديوم 222.
ينتج عن اضمحلال الراديوم إشعاع مؤين يتسبب في توهج المواد الفلورية.
يعود الفضل إلى مدام كوري في اكتشاف الراديوم الذي قدم إسهامات كبيرة في العلوم.
الفرانسيوم هو عنصر مشع يُرمز له بالرمز الكيميائي Fr وعدد ذراته 87. يتكون عن طريق اضمحلال ألفا للأكتينيوم-227 ويمكن العثور عليه بكميات صغيرة في الطبيعة.
وجميع نظائر الفرانسيوم الـ 21 المعروفة حالياً مشعة ولها أنصاف أعمار قصيرة جداً. ومن بين هذه النظائر، يتمتع الفرانسيوم-223 بأطول عمر نصفي يبلغ 21 دقيقة ويبعث جسيمات بيتا. والنظائر الثلاثة الأخرى ذات الأعمار النصفية الأطول نسبياً هي الفرانسيوم-212 والفرانسيوم-222 والفرانسيوم-221، حيث تبلغ أعمارها النصفية 19.3 و14.8 و4.8 دقائق على التوالي.
البولونيوم هو أحد أندر العناصر المعروفة للبشر، ورمزه الكيميائي بو ورقم ذري 84. يبلغ تركيزه في القشرة الأرضية حوالي مائة تريليون ويتم الحصول عليه بشكل أساسي من خلال التخليق الاصطناعي.
ينبعث من معدن البولونيوم الأبيض الفضي اللون توهج في الظلام. وقد اكتشفه العالمان الشهيران مدام كوري وزوجها بيير كوري في عام 1898، وسُمي على اسم موطن مدام كوري في بولندا.
ومن المعروف أيضًا أن البولونيوم من أكثر المواد سمية في العالم.

اليورانيوم هو عنصر عدده الذري 92 ورمزه U. وهو أثقل عنصر موجود بشكل طبيعي.
هناك ثلاثة نظائر لليورانيوم موجودة في الطبيعة، وجميعها مشعة ولها أنصاف أعمار طويلة جدًا، تتراوح بين مئات الآلاف من السنين إلى 4.5 مليار سنة.

البلوتونيوم هو عنصر مشع رقمه الذري 94 ورمزه Pu. وهو مادة خام مهمة لصناعة الطاقة الذرية وله تطبيقات مختلفة، بما في ذلك استخدامه كوقود نووي وكعامل انشطار في الأسلحة النووية. صُنع قلب القنبلة الذرية التي ألقيت على ناغازاكي من البلوتونيوم. تم تصنيع البلوتونيوم لأول مرة في المختبر الوطني الأمريكي في ديسمبر 1940.
الفلزات الحديدية هي فلزات تحتوي على الحديد كمكون رئيسي لها، بينما الفلزات غير الحديدية هي فلزات لا تحتوي على الحديد كمكون رئيسي لها. هذا الاختلاف في التركيب يعطي هذين النوعين من الفلزات خواص وخصائص مختلفة.
المعدن الأكثر استخدامًا في العالم هو الحديد. ويُستخدم الحديد على نطاق واسع في البناء والنقل والتصنيع نظرًا لقوته ومتانته وانخفاض تكلفته. وتشمل المعادن الأخرى الشائعة الاستخدام الألومنيوم والنحاس والصلب.
إن أقوى معدن المعروف حاليًا التنجستنوالمعروف أيضًا باسم ولفرام، بقوة شد تصل إلى 1,510 ميجا باسكال (MPa). ويتمتع التنجستن بأعلى درجة انصهار من أي معدن، بالإضافة إلى مقاومة ممتازة للتآكل، مما يجعله ذو قيمة عالية في مجموعة متنوعة من الصناعات، بما في ذلك الفضاء والدفاع والإلكترونيات. ومع ذلك، هناك مواد أخرى ذات قوة شد أعلى من التنجستن، مثل الأنابيب النانوية الكربونية والجرافين، ولكنها ليست معادن.
أغلى معدن في العالم حاليًا هو الروديوم. فاعتبارًا من مارس 2023، يتم تداول الروديوم بحوالي $20,000 للأوقية الواحدة، مما يجعله أغلى من الذهب بأكثر من 10 أضعاف. الروديوم معدن نادر أبيض فضي اللون يستخدم في المقام الأول في المحولات الحفازة في السيارات والتطبيقات الصناعية الأخرى، وكذلك في المجوهرات وغيرها من عناصر الزينة. وتشمل المعادن الأخرى باهظة الثمن البلاتين والذهب والبلاديوم.
تشمل المعادن المغناطيسية الحديد والنيكل والكوبالت والصلب والصلب المقاوم للصدأ والمعادن الأرضية النادرة. وتُظهِر بعض المواد من بينها مغناطيسية دائمة، في حين لا تُظهِر مواد أخرى، مثل الفولاذ المقاوم للصدأ، مغناطيسية إلا إذا كانت تمتلك تركيبًا كيميائيًا معينًا.
حديد
الحديد هو أقوى المعادن الحديدية المغناطيسية وهو المسؤول عن منح الأرض مجالها المغناطيسي. وهو عنصر أساسي في نواة الكوكب.
نيكل
النيكل أيضًا معدن مغناطيسي شائع ذو خواص مغناطيسية حديدية. لطالما استخدم النيكل في صناعة العملات المعدنية.
كوبالت
الكوبالت هو معدن مغناطيسي حديدي تم استخدامه على نطاق واسع على مدار القرن الماضي نظرًا لخصائصه المغناطيسية الاستثنائية. وهو مناسب لإنتاج كل من المغناطيسات اللينة والصلبة.
الفولاذ
الفولاذ مغناطيسي حديدي بسبب محتواه من الحديد، مما يجعله ينجذب كثيرًا إلى المغناطيس. بالإضافة إلى ذلك، فإن الصلب قادر على إنتاج مغناطيس دائم.
الفولاذ المقاوم للصدأ
الفولاذ المقاوم للصدأ هو سبائك الصلب بإضافة الكروم إلى المزيج. بينما تُظهر بعض أنواع الفولاذ المقاوم للصدأ خواص مغناطيسية، لا تُظهر أنواع أخرى خواص مغناطيسية. وتتأثر الخواص المغناطيسية للفولاذ المقاوم للصدأ الحديدي والمارتنسيتي بتركيبها وبنيتها الجزيئية.
محتوى النيكل هو العامل الأساسي الذي يفسر الاختلافات في الخواص المغناطيسية بين الأنواع المختلفة من الفولاذ المقاوم للصدأ.
المعادن الأرضية النادرة
الفولاذ المقاوم للصدأ عبارة عن سبيكة فولاذ مصنوعة من سبائك الصلب بإضافة الكروم إلى المعدن الأساسي. ومع ذلك، ليست كل أنواع الفولاذ المقاوم للصدأ مغناطيسية، والخواص المغناطيسية للفولاذ المقاوم للصدأ الفولاذ المارتنسيتي المقاوم للصدأ نتيجة لتركيبها الكيميائي وتركيبها الجزيئي.
إن كمية النيكل الموجودة في الفولاذ المقاوم للصدأ هي العامل الأساسي الذي يسبب الاختلافات في خواصه المغناطيسية عبر الأنواع المختلفة من الفولاذ المقاوم للصدأ.
يُظهر عدد محدود فقط من الفلزات في الجدول الدوري خواص مغناطيسية. وعلى النقيض من ذلك، فإن غالبية المعادن الشائعة الاستخدام، مثل الألومنيوم والذهب والفضة والنحاس، غير مغناطيسية.
Aألومنيوم
تتشابه البنية البلورية للألومنيوم مع بنية الليثيوم والمغنيسيوم، وهو ما يجعله غير مغناطيسي. تُصنَّف المواد الثلاث جميعها على أنها معادن شبه مغناطيسية.
Gقديم
على غرار المعادن الأخرى، فإن الذهب ثنائي المغناطيسية، مما يعني أن لديه جاذبية مغناطيسية طفيفة للمغناطيس القوي. وهذه الخاصية شائعة بين جميع المعادن ثنائية المغناطيسية، بما في ذلك الذهب.
Sإيلفر
الفضة معدن آخر غير مغناطيسي. فعدم مغناطيسية الفضة يجعلها غير مغناطيسية.
Cأوبر
النحاس ليس مغناطيسياً بطبيعته، لكنه يمكن أن يتفاعل مع المغناطيس بعدة طرق، بما في ذلك توليد تيارات دوامة. وتستفيد محطات توليد الطاقة من هذه الخاصية للنحاس لتوليد الكهرباء.
تشمل المعادن الثقيلة الزئبق والرصاص والكادميوم والذهب والفضة والنحاس والحديد.
المعادن الثقيلة هي المعادن التي تزيد كثافتها عن 4.5 جم/سم3. وهي شديدة المقاومة للتحلل الأحيائي ويمكن أن تتراكم في السلسلة الغذائية، مما يؤدي إلى إثراء البيئة بمئات الأضعاف.
عندما تدخل المعادن الثقيلة إلى جسم الإنسان عن طريق الغذاء، يمكن أن تعطل الوظائف الفسيولوجية الطبيعية وتشكل تهديدًا لصحة الإنسان. ويشار إلى هذه الأنواع من المعادن الثقيلة باسم المعادن الثقيلة السامة.
فيما يتعلق بالتلوث البيئي، تشير المعادن الثقيلة بشكل أساسي إلى العناصر الثقيلة ذات السمية البيولوجية الكبيرة مثل الزئبق والكادميوم والرصاص والكروم والزرنيخ الفلزي.
للمعادن الثقيلة القدرة على التفاعل بقوة مع البروتينات والإنزيمات داخل جسم الإنسان، مما يجعلها غير نشطة. وعلاوة على ذلك، يمكن أن تتراكم في أعضاء معينة، مما يؤدي إلى التسمم المزمن.
أغلى معدن في العالم هو البلوتونيوم الذي يبلغ سعر الأوقية منه $113400 دولار أمريكي.
البلوتونيوم هو معدن مشع يستخدم في إنتاج كريات الوقود لمحطات الطاقة النووية، بالإضافة إلى أنه عنصر يدخل في صناعة الأسلحة النووية.
لماذا البلوتونيوم مكلف للغاية؟
البلوتونيوم عنصر نادر يوجد عادة بكميات صغيرة داخل خام اليورانيوم في الطبيعة. ومع ذلك، يتم إنتاج معظم البلوتونيوم كمنتج ثانوي لصناعة الطاقة النووية، عن طريق تشعيع اليورانيوم في المفاعلات. وتشير التقديرات إلى أنه يتم توليد حوالي 20 طناً من البلوتونيوم سنوياً من خلال هذه العملية.
ونظراً لتطبيقاته المحدودة، والتي تشمل الطاقة النووية والأسلحة والأبحاث العلمية، والمخاطر المحتملة التي يشكلها على البشر إذا أسيء التعامل معه، يخضع البلوتونيوم للوائح صارمة ويصعب الحصول عليه. بالإضافة إلى ذلك، يمكن أن يكون الحصول عليه مكلفاً للغاية.
الألومنيوم هو العنصر الفلزي ذو أعلى تركيز في القشرة الأرضية، حيث يمثل 7.731 تيرابايت تيرابايت من الإجمالي. الكالسيوم هو العنصر المعدني الذي يحتوي على أعلى تركيز في جسم الإنسان، حيث يشكل 1.51 تيرابايت 3 تيرابايت من تركيبته. والحديد هو المعدن الذي يحتوي حالياً على أعلى إنتاج سنوي على مستوى العالم.
الهيدروجين هو المعدن الأقل كثافة وأصبح أخف المعادن كثافة بعد أن أنتج علماء في جامعة إدنبرة الهيدروجين المعدني للمرة الأولى في يناير 2016. ويتمتع الأوزميوم بأعلى كثافة بين جميع المعادن، حيث تبلغ كثافته 22.48 × 10 كجم/م³.
الكروم هو أكثر الفلزات صلابة مع صلابة موس تبلغ صلابته حوالي 9، في حين أن السيزيوم هو المعدن الأكثر ليونة حيث تبلغ صلابته في موس حوالي 0.5. والفضة هي أكثر الفلزات توصيلًا.
يُعتبر التيتانيوم أهم معدن لتصنيع الطائرات عالية السرعة، ويطلق عليه العلماء اسم "معدن القرن الحادي والعشرين" أو "فولاذ المستقبل". اليورانيوم هو أكبر عنصر مشع موجود في مياه البحر، حيث يقدر إجمالي احتياطيات مناجم اليورانيوم الأرضية بمليوني طن وإجمالي كمية اليورانيوم في المحيطات تقدر بـ4 ملايين طن.
يحتوي القصدير على أكبر عدد من النظائر، حيث يحتوي على 10 نظائر مستقرة، بينما يحتوي الصوديوم على نظير مستقر واحد فقط، وهو Na-23.
الذهب هو المعدن الأكثر مرونة، حيث يمكن تحويله إلى صفائح رقيقة تصل سمكها إلى 10000 مم. أما البلاتين فهو أكثر المعادن قابلية للسحب، ويمكن سحبه إلى أسلاك يصل قطرها إلى 1/5000 مم.
التنجستن له أعلى درجة انصهار من بين جميع المعادن، حيث تبلغ درجة انصهاره 3410 ℃، بينما الزئبق له أقل درجة انصهار، حيث ينصهر عند -38.8 ℃. الجاليوم له أكبر فرق بين درجة انصهاره (30 ℃) ودرجة غليانه (2403 ℃). ويمتلك الفرانسيوم أقل تركيز في القشرة الأرضية، حيث يبلغ محتواه 37 فقط لكل طن × 10-13 جم، أو حوالي 1 × 10-211 تيرابايت 3 تيرابايت.
السيزيوم هو المعدن الأكثر استجابة للضوء ويولد أكبر تيار. فعندما يضيء سطحه، يمكن للإلكترونات أن تكتسب الطاقة وتخرج من السطح، مما يؤدي إلى توليد تيار كهروضوئي. يتمتع السيزيوم أيضًا بأكبر الخواص الفلزية بين جميع الفلزات.
يُعد الكالورنيوم أغلى معدن في العالم، حيث يبلغ سعره 1 تيرابايت و10 ملايين دولار أمريكي للغرام الواحد، مما يجعله أغلى من الذهب بأكثر من 500,000 مرة. الحديد هو المعدن الأقل تكلفة.
النيوبيوم هو العنصر الأكثر عملية في التوصيل الفائق، حيث يصبح موصلًا فائقًا بدون مقاومة تقريبًا عند تبريده إلى -263.9 ℃. ويتمتع البلاديوم بأكبر قدرة على امتصاص الغاز، حيث يمكن لحجم واحد من البلاديوم الغروي امتصاص ما يصل إلى 1200 حجم من الهيدروجين.
ليس من الممكن دائمًا معرفة ما إذا كان المعدن سامًا بمجرد النظر إليه أو التعامل معه. فبعض المعادن يمكن أن تكون سامة في أشكال معينة أو بتركيزات معينة، في حين أن البعض الآخر قد لا يكون سامًا على الإطلاق.
وتعتمد سمية المعدن على عوامل مثل شكل المعدن (مثل المادة الصلبة أو السائلة أو الغازية)، والتركيز أو جرعة التعرض، ومسار التعرض (مثل الاستنشاق، الابتلاع، ملامسة الجلد).
لتحديد مدى سمية المعدن، من المهم الرجوع إلى مصادر موثوقة مثل صحيفة بيانات سلامة المواد (MSDS) أو غيرها من إرشادات السلامة. ستوفر هذه المصادر معلومات عن المخاطر والاحتياطات المرتبطة بالمعدن، بالإضافة إلى إرشادات المناولة الآمنة والتخزين والتخلص الآمن.
من المهم أيضًا اتباع إجراءات السلامة السليمة عند التعامل مع أي معدن، مثل ارتداء معدات واقية مثل القفازات والنظارات الواقية وأجهزة التنفس، وتجنب التلامس المباشر مع المعدن كلما أمكن ذلك.
من بين 118 عنصرًا معروفًا في الجدول الدوري، يُعتبَر حوالي 90 عنصرًا فلزًّا. ويعتمد العدد الدقيق على كيفية تصنيف بعض العناصر الحدية (ذات الخصائص الفلزية واللافلزية).